
搜索网站、位置和人员

电话: +86-(0)571-86886861 公共事务部
诺维氏梭菌是一种厌氧、产芽孢的革兰氏阳性细菌,可机会性地侵入人和其他动物体内,造成包括气性坏疽、肌炎、坏死性肝炎和脓毒症等在内的多种重症感染。诺维氏梭菌的外毒素alpha-toxin(Tcnα)是该菌最重要的毒力因子,所有致病性的诺维氏梭菌菌株均表达Tcnα 1。Tcnα属于大梭菌毒素家族,但 Tcnα与该毒素家族其他成员差异显著,也是唯一专性使用尿苷二磷酸-N-乙酰葡糖胺为辅酶的大梭菌毒素2。
2021年5月10日,西湖大学生命科学学院的陶亮研究员以通讯作者在《Cell Research》上在线发表了题为“Sulfated glycosaminoglycans and low-density lipoprotein receptor mediate the cellular entry of Clostridium novyi alpha-toxin”的研究论文,首次揭示了硫酸化糖胺聚糖分子和低密度脂蛋白受体是Tcnα入侵宿主的细胞受体,并阐明其在毒素破坏肌组织过程起到重要的介导作用。本研究阐示了诺维氏梭菌感染后毒素作用机制,并为该类感染疾病的防治提供了新策略。
西湖大学生命科学学院陶亮团队的博士生周瑶、李谛音和博士后罗建华为本文的共同第一作者,西湖大学生命科学学院的陶亮研究员为通讯作者。
论文链接:https://www.nature.com/articles/s41422-021-00510-z

在本研究中,研究者首先利用异源表达后纯化的Tcnα在CRISPR/Cas9全基因组水平的敲除文库上进行了多轮压力选择,进行高通量测序分析后发现:多个靶向硫酸化糖胺聚糖生物合成途径相关基因的向导RNA(gRNA)在筛选后文库中得到高度富集(图1)。
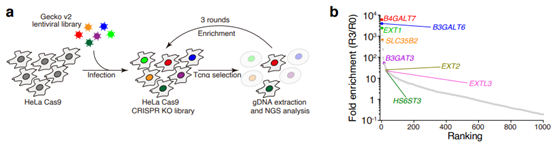
图1:全基因组的CRISPR/Cas9系统介导的基因敲除库筛选Tcnα在细胞中潜在的受体及毒素作用相关的宿主蛋白
之后研究者通过一系列生化和细胞学实验,包括构建敲除和补回细胞株、体外结合、竞争拮抗等验证了细胞表面的硫酸化糖胺聚糖可被Tcnα识别,进而使Tcnα在细胞表面的聚集。硫酸化糖胺聚糖和低密度脂蛋白受体(LDLR)家族成员经常协同作用介导配体的入胞过程,而这一途径也常被许多病原体所劫持利用,包括丙肝病毒和艰难梭菌毒素A等 3。本研究发现Tcnα也可以利用类似的方式入胞,Tcnα首先被细胞表面丰富的硫酸化糖胺聚糖捕获,然后递送给LDLR并由后者介导高效的内吞入胞过程(图2)。

图2: Tcnα结合硫酸糖胺聚糖后在细胞表面富集,而低密度脂蛋白受体介导了毒素的高效入胞。
气性坏疽和肌炎是诺维氏梭菌感染的典型症状,表现包括肌肉和皮下组织充斥炎性组织液渗出以及明显的组织急性坏死4。研究者通过小鼠胫前肌肌注Tcnα来模拟这一病理过程的发生:肌肉Tcnα注射可造成明显的组织损伤,表现为肿胀、出血、炎性细胞浸润和肌细胞细胞核中位(肌肉细胞病变坏死的早期标志)。硫酸环糊精作为硫酸化糖胺聚糖类似物,同时具有低细胞和组织毒性和溶血性,被认为是一种有价值的药物分子。研究者发现同时注射硫酸环糊精可以竞争性地拮抗毒素与宿主细胞的结合,从而显著减轻Tcnα所造成的肌病理症状(图3)。
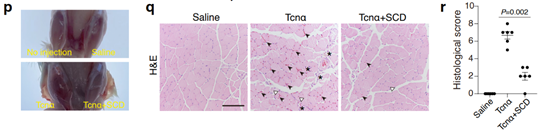
图3:小鼠肌注Tcnα后诱导显著的肌组织损伤,同时注射硫酸环糊精可抑制症状的发生。
西湖大学陶亮课题组同时还受到西湖实验室和浙江省结构生物学研究重点实验室的支持。实验室主要从事病原微生物和宿主之间的相互作用的研究,包括从分子、生化、细胞、结构、组学等方面研究病原体及其效应蛋白对重要细胞功能的影响及作用机制,并针对微生物感染问题开展相应的工程和转化研究。实验室招收分子生物学、微生物学、细胞生物学、生化和结构生物学、免疫学、生物信息学、遗传和实验动物学等方向的科研助理和博士后,热忱欢迎加盟。简历和相关材料请投递至:taoliang@westlake.edu.cn。
参考文献
1 Hatheway CL. Toxigenic clostridia. Clin Microbiol Rev 1990; 3:66-98.
3 Tao L, Tian S, Zhang J et al. Sulfated glycosaminoglycans and low-density lipoprotein receptor contribute to Clostridium difficile toxin A entry into cells. Nat Microbiol 2019.
4 Aronoff DM, Kazanjian PH. Historical and contemporary features of infections due to Clostridium novyi. Anaerobe 2018; 50:80-84.
最新资讯
大学新闻
学术研究
学术研究
学术研究
学术研究

















